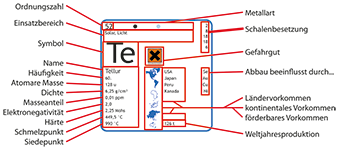
Über Zink » Einsatzgebiete
Im Jahr 2018 wurden über 13,5 Millionen Tonnen Zink produziert. Davon wurden 47 % für den Korrosionsschutz von Eisen- und Stahlprodukten durch Verzinken genutzt. Nach Verbrauchsmengen bedeutendstes Einsatzgebiet sind dessen Legierungen, vorzugsweise solche mit Kupfer, wie Messing, oder mit Aluminium, entweder als AlZn-Legierung oder mit deutlich höheren Zinkgehalten als Alzen, das für im Sandguss und Kokillenguss hergestellte Teile verwendet wird. Auch in den genormten Magnesiumlegierungen ist Zink mit bis zu 5 % enthalten. Ungleich bedeutender sind die genormten Feinzink-Gusslegierungen, die überwiegend im Druckgießverfahren, aber auch in Sand und Kokille vergossen werden. Auch zu Walzmaterial wie Zinkblechen werden Zinklegierungen verarbeitet.
Korrosionsschutz
Zink wird seit langem als Korrosionsschutz (Rostschutz) für Stahl- und Eisenteile verwendet, indem man sie verzinkt, d. h. mit einem metallischen Überzug aus Zink überzieht. Das Zink schützt aktiv und passiv gegen Korrosion, d. h., es bildet einerseits eine Barriere und schützt andererseits auch freiliegende benachbarte Eisenflächen sowie Schichtfehler vor Korrosion, indem es wie eine Opferanode wirkt.
Die Verzinkung kann auf verschiedene Weisen erfolgen. Methoden sind das Feuerverzinken, die galvanische Verzinkung, mechanische Beschichtungen, Spritzverzinken und Zinklamellenüberzüge. Sie unterscheiden sich in der Art des Aufbringens der Zinkschicht, der Dicke und damit der Haltbarkeit.
Die älteste Verzinkungsmethode ist das diskontinuierliche Feuerverzinken (Stückverzinken). Dabei werden vorbehandelte und vorgefertigte Bauteile aus Stahl (z. B. Balkongeländer) in ein Bad mit flüssigem Zink getaucht. In den 1930er Jahren kam als Verfahrensvariante das kontinuierliche Feuerverzinken (Bandverzinken) erstmals zur Anwendung, bei dem Bänder aus Stahl im Durchlaufverfahren als Halbzeug verzinkt und danach erst weiterverarbeitet werden. Durch Stückverzinken entstehen Zinkschichten, die in der Regel zwischen 50 und 150 µm liegen und abhängig von den atmosphärischen Bedingungen für Jahrzehnte vor Korrosion schützen. Bandverzinkte Bleche weisen sehr dünne Zinkschichtdicken zwischen 7 und 25 µm auf und erreichen deshalb nur deutlich kürzere Schutzzeiträume. Die Schutzdauer von feuerverzinktem Stahl kann durch eine zusätzliche Beschichtung (Duplex-System) weiter gesteigert werden.
Beim galvanischen Verfahren wird die Zinkschicht elektrolytisch aufgebracht. Dazu wird das Werkstück gemeinsam mit einem Stück reinem Zink in eine saure oder basische Lösung eines Zinksalzes getaucht. Danach wird Gleichspannung angelegt, wobei das Werkstück die Kathode, das Stück Zink die Anode bildet. Am Werkstück wird durch Reduktion von Zinkionen Zink gebildet. Gleichzeitig wird das reine Zink der Anode oxidiert, die Anode löst sich dabei auf. Es entsteht eine dichte Zinkschicht, die in der Praxis 2,5 bis zu 25 µm. beträgt und somit deutlich geringer ist als beim diskontinuierlichen Feuerverzinken. Die Zinkschicht könnte theoretisch beim galvanischen Verfahren auch auf die Dicke einer feuerverzinkten Schicht gebracht werden. Allerdings wäre das nicht mehr wirtschaftlich aufgrund der Dauer (ca. 0,5 µm in einer Minute) und der Energiekosten.
Beim Spritzverzinken wird das Zink geschmolzen und dann mit Hilfe von Druckluft auf das Werkstück aufgesprüht. Die thermische Belastung ist dabei geringer als beim Feuerverzinken. Das kann für empfindliche Werkstoffe wichtig sein. Wird das Zink mechanisch auf das Werkstück aufgetragen, spricht man vom Plattieren. Ein Verfahren, das für Verzinken von Kleinteilen, etwa Schrauben, angewendet wird, ist das Sherardisieren. Dabei entsteht die Zinkschicht durch Diffusion von Zink in das Eisen des Werkstücks. Eine weitere mögliche Auftragungsart von Zinkschichten sind Zinksprays.
Zink wird als Opferanode zum Schutz größerer Stahlteile genutzt. Dabei wird das zu schützende Objekt leitend mit dem Zink verbunden. Es entsteht eine galvanische Zelle mit Zink als Anode und dem Objekt als Kathode. Da nun das unedle Zink bevorzugt oxidiert wird und sich dabei langsam auflöst, bleibt das Stahlteil unverändert. Solange Zink vorhanden ist, ist somit das Stahlstück vor Korrosion geschützt.
Aufgaben des Korrosionsschutzes haben auch die Weiß- und Farbpigmente auf Basis von Zinkverbindungen. Zinkverbindungen sind auch Bestandteil der Phosphatierungsmittel (Phosphatierung), die Verfahren wie das Bondern von Blechen erst ermöglichen.
Zink in Batterien
Metallisches Zink gehört zu den wichtigsten Materialien für negative Elektroden (Anoden) in nicht wiederaufladbaren Batterien und wird in großtechnischem Maßstab eingesetzt. Beispiele sind Alkali-Mangan-Batterien, Zink-Kohle-Batterien, Zink-Luft-Batterien, Silberoxid-Zink-Batterien und Quecksilberoxid-Zink-Batterien. Zink wurde auch als Anode in vielen historischen galvanischen Elementen verwendet. Dazu zählen unter anderen die Voltasche Säule, das Daniell-Element und das Bunsen-Element. In geringem Umfang wird Zink auch für negative Elektroden in Akkumulatoren (wiederaufladbaren Batterien) verwendet.
Der Grund für die vielfältige Verwendung von Zink in Batterien liegt in der Kombination von physikalischen und elektrochemischen Eigenschaften mit guter Umweltverträglichkeit und relativ niedrigen Kosten. Zink ist ein gutes Reduktionsmittel mit hoher theoretischer Kapazität (0,82 Ah/g). Aufgrund des niedrigen Standardpotenzials von etwa −0,76 V beziehungsweise in alkalischem Medium −1,25 V lassen sich relativ hohe Zellspannungen realisieren. Ferner hat Zink eine gute elektrische Leitfähigkeit und ist in wässrigen Elektrolytlösungen ausreichend stabil.
Um die Korrosion von Zink in der Batterie zu reduzieren und zur Verbesserung der elektrochemischen Eigenschaften wurde früher amalgamiertes Zink mit einem Quecksilbergehalt von bis zu 9 Prozent eingesetzt. Aus Umweltschutzgründen wurde diese Praxis zumindest in Industrieländern nahezu vollständig eingestellt. Im Jahr 2006 wird amalgamiertes Zinkpulver nur noch in Zink-Luft- und Silberoxid-Zink-Knopfzellen verwendet.
Die Anode in Zink-Kohle-Batterien hat die Form eines Zinkbechers. Die Becher werden durch mehrstufiges Tiefziehen aus Zinkblech oder durch schlagartige Verformung (englisch impact extrusion) von runden oder sechseckigen Scheiben aus dickem Zinkblech (sogenannten Kalotten) hergestellt. Zur Verbesserung der Formbarkeit und zur Hemmung der Korrosion enthält das dafür verwendete Zink geringe Mengen an Cadmium, Blei und/oder Mangan. In Alkali-Mangan-Batterien wird Zinkpulver als aktives Material in der Anode verwendet. Es wird meist durch Verdüsung von geschmolzenem Zink im Luftstrahl hergestellt. Zur Hemmung der Korrosion werden dem Zink geringe Mengen anderer Metalle beigemischt, z. B. Blei, Bismut, Indium, Aluminium und Calcium.
Zinkblech im Bauwesen
Wichtige Zinkprodukte sind auch Halbzeuge, meist in Form von Blechen aus legiertem Zink / Titanzink. Titanzinkblech wird als Werkstoff im Bauwesen verwendet. Heute kommt fast ausschließlich Titanzink zum Einsatz, das korrosionsfester, weniger spröde und dadurch mechanisch deutlich belastbarer ist als unlegiertes Zink bzw. das bis in die 1960er Jahre übliche Zinkblech, dass im sogenannten Paketwalzverfahren hergestellt wurde. Gewalztes, massives Titanzinkblech wird hauptsächlich zur Dacheindeckung, als Fassadenbekleidung, für die Dachentwässerung (Regenrinnen, Fallrohre), für Abdeckungen z. B. von Gesimsen oder Außenfensterbänken oder für Anschlüsse und Dachkehlen eingesetzt. Es hält bis zu 100 Jahre und muss in dieser Zeit weder gewartet noch repariert werden, wenn es fachgerecht verarbeitet wurde. Die Verarbeitung erfolgt durch das Klempnerhandwerk.
Zinkblech sollte nicht verwechselt werden mit feuerverzinktem Stahlblech, das fälschlicherweise auch des Öfteren Zinkblech oder Weißblech genannt wird.
Legiertes Zinkblech wird in Coils oder in Tafeln geliefert. Für die Dachdeckung werden oft Metallbahnen (Schare) verwendet, die zwischen 40 und 60 Zentimeter breit sind und bis zu 16 Meter lang sein können. Die Materialdicke ist unterschiedlich, meist beträgt sie 0,7 Millimeter. Die Verbindung der einzelnen Blechteile erfolgt bei kleinteiligen Elementen meist durch Löten, bei Dachdeckungen meist durch doppeltes Falzen (Doppelstehfalzdeckung). Aufgrund der Wärmeausdehnung von legiertem Zink von 22·10−6/K müssen die Verbindungen und Anschlüsse der Zinkprofile Materialbewegungen zulassen.
Moderne Architekten verwirklichen mit Titanzink extravagante Ideen. Daniel Libeskind hat z. B. das Jüdische Museum Berlin oder die Libeskind-Villa in Datteln mit einer Fassade aus Bauzink ausgestattet. Zaha Haddid wählte den Werkstoff für das Transport Museum in Glasgow, das die Verformungseigenschaften des Werkstoffes eindrucksvoll zeigt.
Zinkdruckguss
Zinkdruckguss ist die gebräuchliche Bezeichnung für im Druckgießverfahren hergestellte Teile aus Feinzink-Gusslegierungen. Diese Legierungen erbringen weitaus bessere Werte der Gussteile, als es beim Vergießen von reinem Zink möglich ist. Die Legierungen sind genormt. Viel verwendet wird die Legierung GD ZnAl4Cu1 (Z 410). Zinkdruckguss ermöglicht – wie jedes Druckgießverfahren – die Fertigung großer Stückzahlen. Die Gussteile zeichnen sich durch hohe Maßhaltigkeit aus, besitzen sehr gute mechanische Werte und sind für eine Oberflächenbehandlung wie Vernickeln oder Verchromen gut geeignet. Das Spektrum der Anwendungen umfasst Automobil-Zubehörteile und solche im Maschinen- und Apparatebau, ferner Beschläge aller Art, Teile für die Sanitärindustrie, für Feingeräte- und Elektrotechnik, für Metallspielwaren und viele Gebrauchsgegenstände im Haushalt.
Münzprägung
Da Zink als Münzmetall vergleichsweise wenig kostet, wurde es in Notzeiten, zuletzt in den beiden Weltkriegen, in Form von Zinklegierungen zur Münzprägung verwendet, teilte sich diese Verwendung als sog. „Kriegsmetall“ aber mit Münzen aus einer Aluminiumlegierung. Seit 1982 besteht auch der US-Cent (Penny) im Kern aus Zink.
Analytik
Analysenreines Zinkpulver dient als Urtitersubstanz nach Arzneibuch zur Einstellung von EDTA-Maßlösungen.
Organische Chemie
In der Organischen Synthese dient Zink verschiedenen Zwecken. So fungiert es als Reduktionsmittel und kann als solches in unterschiedlicher Weise aktiviert sein. Ein Beispiel ist die Clemmensen-Reduktion von Carbonylverbindungen mit amalgamiertem Zink. Des Weiteren lassen sich Allylalkohole zu Alkenen reduzieren, Acyloine zu Ketonen. Die Reduktion der aromatischen Nitrogruppe kann in Abhängigkeit von den Reaktionsbedingungen zu unterschiedlichen Produkten führen: Arylamin, Arylhydroxylamin, Azoaren, N,N’-Diarylhydrazin.
Im metallorganischen Bereich bieten Zinkorganyle gegenüber Grignard-Verbindungen Selektivitätsvorteile, da sie in der Regel weniger reaktiv sind und mehr funktionelle Gruppen tolerieren – ein Umstand, von dem die Reformatzki-Reaktion Gebrauch macht. Die Organyle lassen sich auf direkte Weise oder durch Transmetallierung herstellen. In Gegenwart asymmetrisch komplexierender Auxiliare, von denen mitunter katalytische Mengen ausreichen, ist eine stereoselektive Addition möglich. Der Effekt der Chiralitätsverstärkung wurde beobachtet.
Nicht zuletzt ist die Halogeneliminierung und Dehalogenierung möglich. Die Simmons-Smith-Reaktion zählt zu den selteneren Präparationsmethoden. Die Zeitschrift Organic Syntheses verzeichnet eine Reihe von Synthesen, in denen elementares Zink als Reagenz dient.
Herstellung von Wasserstoff
Zink wird im sogenannten Solzinc-Verfahren zur Herstellung von Wasserstoff genutzt. Dafür wird in einem ersten Schritt Zinkoxid thermisch durch Sonnenenergie in Zink und Sauerstoff aufgespalten, und in einem zweiten Schritt wird das so gewonnene Zink mit Wasser zu Zinkoxid und Wasserstoff umgesetzt.